morfologi
Pada tahap makroskopik, tahap atropi kortikal yang berlainan (pengurangan tisu atau massa organ) dapat dilihat pada penyakit Alzheimer, yang ditandai dengan pembesaran kelenjar parietal, lebih menonjol dalam cuping depan, temporal dan parietal. Atrofi ini dikompensasi oleh pembesaran rongga ventrikel sekunder dengan kehilangan parenchyma (angka 1). Secara khususnya, dalam peringkat lanjut penyakit, struktur lobus temporal medial, termasuk hippocampus, korteks entorhinal dan amygdala, atrophy teruk, diberikan penglibatan mereka bermula dari peringkat awal patologi.
Tambahan pula, penyakit Alzheimer juga menyampaikan perubahan mikroskopik, yang dikenali sebagai plak sengaja ekstraselular dan kluster neurofibrillari intraselular, yang merupakan asas diagnosis histologi. Dengan perkembangan penyakit tersebut, maka terdapat kerugian neuron yang serius yang disertai dengan gliosis (percambahan atau pembiakan yang meresap, bersifat reaktif, sel-sel neuroglia, iaitu sel-sel yang membentuk stroma sokongan tisu saraf) di kawasan yang sama di mana kehadiran plak dan kluster neurofibrillary lebih besar.
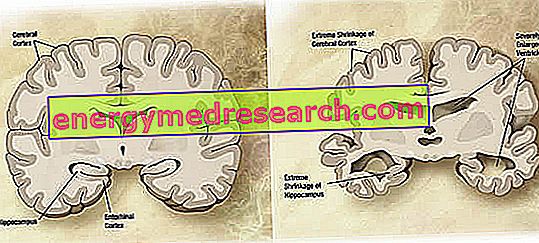
Rajah 1. Bahagian otak dalam otak: perbezaan antara otak dan otak biasa yang dipengaruhi oleh AD (sumber imej wikipedia).
patogenesis
Penyakit Alzheimer dicirikan terutamanya oleh dua luka biasa: pengumpulan ekstraselular plak sengaja yang terdiri terutamanya daripada peptida β-amyloid (Aβ) dan kluster neurofibrillari intraneuronal, dibentuk oleh protein tau hyperphosphorylated.
- Plak senaman boleh didapati di peringkat kawasan otak seperti hippocampus, amygdala dan neocortex.
Peptida Aβ berasal dari potongan proteolitik dari prekursor protein amiloid (APP), oleh β-secretase. Potongan ini menghasilkan fragmen carboxy terminal dari 99 sisa (CTF atau C99) yang kemudian dipotong oleh β-secretase untuk menghasilkan serpihan Aβ, yang mempunyai panjang yang berbeda. Adalah diketahui bahawa spesies Aβ yang paling banyak adalah fragmen Aβ40. Satu lagi serpihan yang diketahui terbentuk daripada potongan proteolitik, kurang banyak daripada Aβ40, adalah Aβ42, lebih mudah untuk membentuk fibril amiloid, yang berkumpul sebagai spesimen Aβ di otak individu dengan penyakit Alzheimer.
- Komponen lain yang hadir dalam penyakit Alzheimer diwakili oleh kelompok neurofibrillari yang terdiri daripada berkas-berkas filamen yang terdapat dalam sitoplasma neuron. Klaster neurofibrillary tidak dapat diselesaikan dan kelihatannya tahan terhadap proses proteolisisis dalam vivo, dan seterusnya tinggal di bahagian tisu walaupun lama selepas kematian neuron. Melihat struktur, kluster fibrillar terdiri daripada filamen helix berganda dan filamen linear komposisi serupa. Menganalisis komposisi, helix double helix kebanyakannya terbuat dari protein tau hyperphosphorylated. Tau adalah protein akson yang dikaitkan dengan microtubules yang memudahkan perhimpunannya.
Perubahan penting neuropatologi lain yang terdapat dalam penyakit Alzheimer termasuk disfungsi mitokondria, kerosakan neuron oksidatif, kehilangan sinaptik dan degenerasi aksonal.
Aspek neurokimia
Seperti yang telah dijelaskan, peptida Aβ, yang berasal dari potongan proteolitik dari prekursor APP, mewakili komponen neurotoksik penyakit Alzheimer . Khususnya, ia telah dihipotesiskan bahawa Aβ mungkin penting untuk fungsi otak normal dan, jika ia mengatasi kepekatan tertentu, ia mungkin menjadi neurotoksik. Di samping itu, kedua-dua agregat dan pelbagai isoforms Aβ boleh mempunyai peranan biologi, fisiologi atau patologi yang berbeza, menentukan dan mengambil bahagian dalam peringkat seterusnya penyakit ini. Telah diperhatikan bahawa Aβ bertindak sebagai neuromodulator, mempengaruhi pembebasan beberapa neurotransmiter jika tidak ada tanda-tanda neurotoxicity yang jelas.
Sebagai contoh, peranan neuromodulator Aβ, dalam konteks fisiologi, boleh mempunyai makna yang penting untuk keseimbangan sistem neurotransmitter yang betul. Sudah diketahui bahawa sistem ini terdiri daripada neurotransmitter, bahan yang menyampaikan maklumat antara sel-sel yang membentuk sistem saraf, neuron, melalui transmisi sinaptik.
Dalam keadaan patologi, di sisi lain, transmisi sinapsik Aβ-mediated boleh dikaitkan dengan perubahan neurotransmitasi sebelum peristiwa neurodegenerative. Akibat perubahan ini, gangguan awal kognitif dan bukan kognitif mungkin timbul, berdasarkan sistem neurotransmitter yang terjejas dan kawasan otak yang berbeza terlibat.
Perubahan sistem neurotransmitter dan mekanisme transduksi isyarat dalam otak individu yang menderita penyakit Alzheimer sangat kompleks. Salah satu sistem yang nampaknya diubah ialah sistem isyarat cholinergik, yang melibatkan asetilkolin neurotransmitter. Sesungguhnya, ia telah menunjukkan bahawa individu yang menderita penyakit Alzheimer menunjukkan penurunan penghantaran cholinergik pada tahap korteks dan hippocampus, kawasan otak penting yang didedikasikan untuk fenomena seperti pembelajaran dan ingatan. Sebagai tambahan kepada sistem neurotransmitter ini, perubahan dalam sistem noradrenergik, serotonergik, serta glutamat dan sistem GABA telah diperhatikan dalam penyakit Alzheimer.