2, 3 diphosphoglycerate (2, 3 DPG) adalah sebatian yang diperoleh daripada produk perantaraan glikolisis; ia menumpu terutamanya pada tahap erythrocyte, kerana sel darah merah - yang tidak mempunyai mitokondria - mengeksploitasi metabolisme laktat anaerobik (penapaian homolaktik glukosa) untuk mendapatkan tenaga.
Hemoglobin adalah protein tetramerik, iaitu, dibentuk oleh empat subunit, dua alpha dan dua beta, masing-masing terdiri daripada bahagian protein (globin) dan EME (kumpulan prostetik yang mengikat oksigen). 2, 3-diphosphoglycerate melekat pada rantai Beta dengan memampatkannya dan mengurangkan pertalian hemoglobin untuk oksigen.
Pengikatan 2, 3 DPG ke hemoglobin terjadi apabila ia berada dalam bentuk deoksigenasi, sementara itu dibubarkan di paru-paru dari pengikatan hemoglobin menjadi oksigen. Malah apabila hemoglobin mencapai tisu, rantai β adalah yang pertama untuk menyerahkan oksigen dan kehilangan ini melibatkan pemindahan monomer dari pusat. Sebagai rongga hidrofilik dalaman membuka DPG memasuki dan mengikat tetramer yang membentuk ikatan heteropolar antara kumpulan-kumpulan yang bermuatan negatif, dan residu lisin dan histidin rantai beta, dikenakan secara positif. Struktur yang begitu stabil juga boleh melepaskan oksigen rantai dua α. Dalam paru-paru, bagaimanapun, proses sebaliknya berlaku; pada tekanan oksigen yang tinggi rantai α adalah yang pertama untuk mengikatnya dan DPG adalah "diperah" dan dikeluarkan dari tetramer, yang membolehkan ikatan Rantai Oksigen yang lebih mudah.
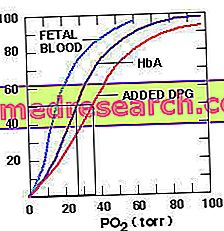
2, 3-bisphosphoglycerate tidak boleh mengikat hemoglobin janin, kerana molekul ini tidak mempunyai rantai B dengan 2.3 DPG menarik sambungannya. Ini menjelaskan pertalian yang lebih besar untuk oksigen hemoglobin janin berbanding dengan hemoglobin ibu, ciri yang membolehkan darah janin untuk mengeluarkan oksigen dari darah ibu.



